
一、病历摘要
患者56岁女性,主因“间断胸闷、憋气1年余”入院。患者5年前因急性心肌梗死,三支病变行冠状动脉旁路移植手术,搭桥4根(LIMA-LAD,其他为静脉序贯吻合桥)。1年前平卧休息时出现胸闷、憋气,伴干咳,行冠脉造影检查,桥血管均通畅,发现主动脉瓣狭窄,给予药物治疗。4月前患者胸闷气短症状加重。我院查超声心动图示:主动脉瓣重度狭窄,轻-中度关闭不全;)二尖瓣轻-中度关闭不全;三尖瓣中量反流,左室射血分数减低。进行住院治疗。
既往史:高血压、2型糖尿病、高脂血症8年。
体格检查:心率:80次/分,血压:左上肢95/58mmHg,右上肢97/57mmHg,左下肢137/91 mmHg,右下肢血压未测出,体弱,双肺呼吸音粗,双下肺可闻及小水泡音。心律齐,主动脉瓣第一听诊区可闻及收缩期3/6级喷射性杂音,向右锁骨下传导。双下肢无可凹性水肿。
辅助检查:
心电图:
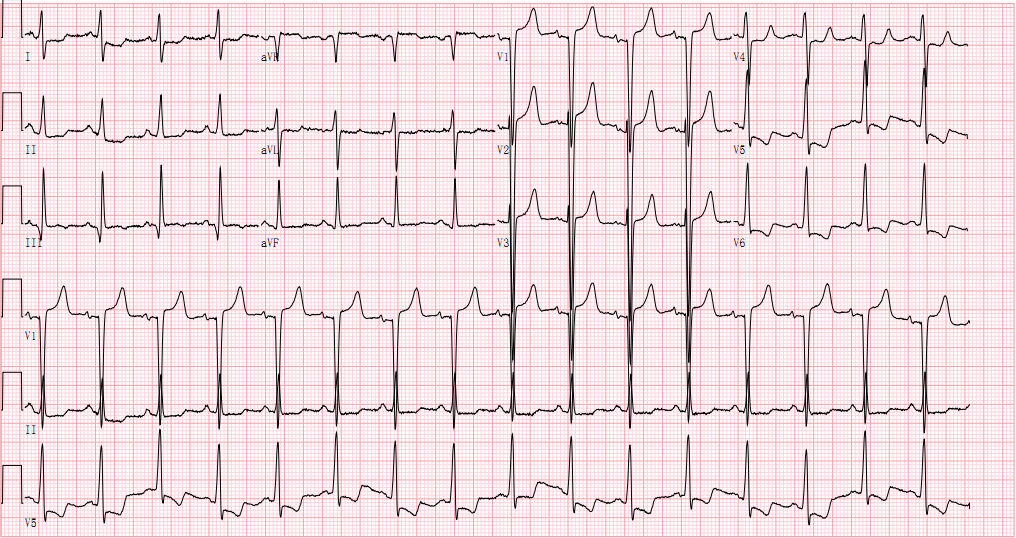
窦性心律,左室高电压,ST-T改变。
胸部X线:
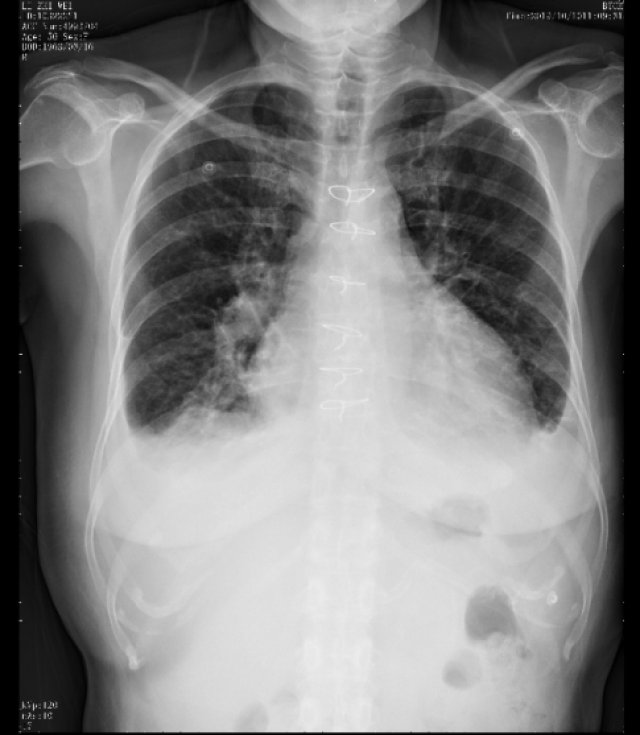
双肺渗出,心影增大,心胸比:0.60,双侧胸腔积液。
超声心动图:
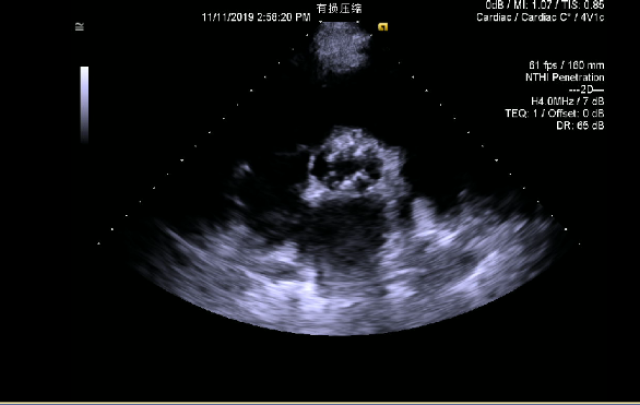
左心增大,室间隔增厚,左室心尖部小室壁瘤形成,大小约15x12mm;主动脉瓣病变,二叶瓣不除外,重度狭窄(跨瓣压差58mmHg),轻-中度关闭不全;二尖瓣钙化,轻-中度关闭不全;三尖瓣中-大量反流,肺动脉收缩压增高,估测肺动脉收缩压约为52mmHg。主动脉瓣Vmax:510cm/s,左室射血分数减低,左室舒张末径: 59 mm,左室射血分数: 24 %。
主动脉根部CTA:
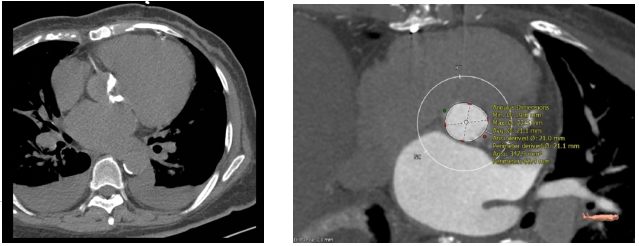
主动脉二叶式畸形,瓣膜增厚,存在重度钙化,分布于两个瓣叶游离缘。主动脉瓣环周长折算直径21.1mm
冠脉造影:
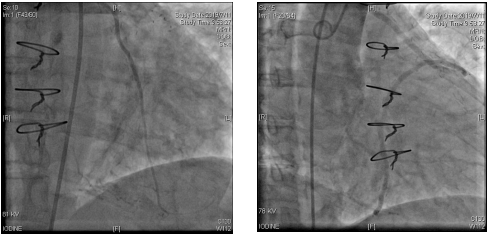
LIMA-LAD桥血管通畅,升主动脉造影显示:AO-SVG-D1-LCX-RCA桥血管通畅。
二、临床决策
1.临床诊断:主动脉瓣狭窄(重度),二尖瓣少-中量反流,三尖瓣关闭不全(重度),心脏扩大,心功能IV级。
2.治疗方案选择:
患者主动脉瓣重度狭窄伴中度反流诊断明确,目前患者胸闷症状明显,心功能IV级,病情分级为Stage D期,EUROScore I评分14分,为主动脉瓣置换手术适应症,可选方式包括SAVR和TAVI(2017年 AHA/ACC I,A类推荐),但因患者5年前曾行冠状动脉搭桥术,近期冠脉造影提示桥血管通畅,结合该患者整体评估情况,实施常规再次开胸行主动脉瓣手术风险较高,且二次开胸有损伤目前仍通畅的桥血管风险,故确定将TAVI作为该患者的首选手术方式。
TAVI目前常用入路有两种,经心尖及经股动脉,对于该患者,入院后查体发现右下肢血压不能测出,行超声检查提示双侧下肢粥样硬化斑块狭窄,经外周置入人工瓣膜时难度较大并可能导致斑块脱落,而经心尖部入路可避免此风险。由主动脉CTA评估患者左心室流出道无狭窄,主动脉瓣投射角度可,遂决定拟行经心尖部TAVI手术。
3.手术时机:
患者入院后经积极的药物治疗,胸闷憋气症状无明显缓解,活动耐量逐渐下降,精神状态渐弱,且双侧胸腔积液较入院明显增多,予患者双侧胸腔穿刺每日可放出积液500~800ml。种种迹象表明,患者内科保守治疗无效,急需手术治疗,我科与心脏内科、麻醉科、导管室、手术室多科会诊后共同决定尽快行TAVI治疗。
4.手术策略及过程:
瓣膜选择:根据患者主动脉CTA重建图像,确定患者适用21# J-Valve自膨胀生物瓣膜
备选方案:因患者为高危患者,术中湿备体外循环,如TAVI手术失败,紧急行体外循环下正中切口主动脉瓣置换术。
患者TAVI手术过程平稳,历时2小时43分钟,出血10ml。
术后1月患者回院复查,自诉可正常进行日常家务,胸闷憋气症状基本消失。
胸部X线:
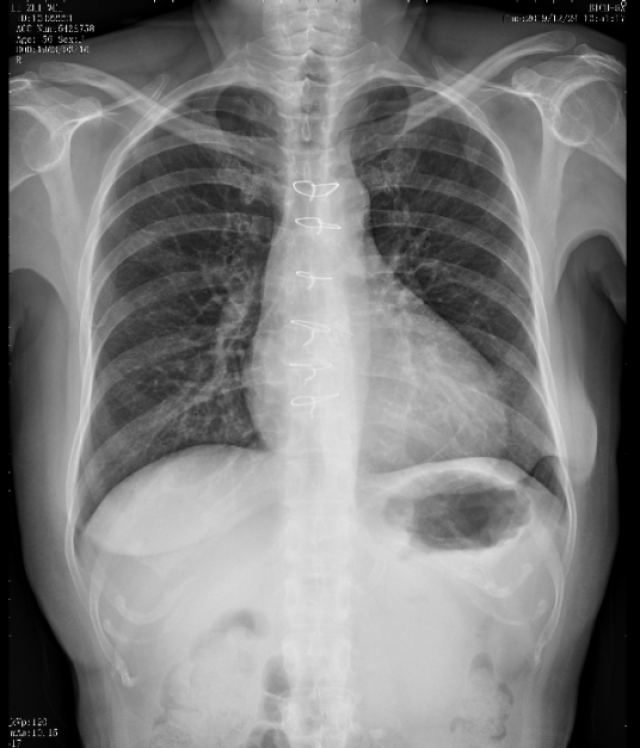
双肺渗出较前明显减少,心胸比:0.53,双侧胸腔积液消失。
超声心动图:
人工瓣功能正常,左室射血分数:46%,左室舒张末径:54mm。主动脉瓣Vmax:230cm/s,二尖瓣少量反流;三尖瓣少量反流。
三、讨论与总结
1.主动脉瓣狭窄需要手术干预的适应症?
2017年AHA/ACC瓣膜病指南指出,主动脉狭窄的外科治疗绝对适应症为:(1)有临床症状的高压差重度AS或运动试验时出现症状。(2)无临床症状的重度AS,但EF<50%。(3)重度AS患者同时须行其他心脏手术(如CABG)
主动脉狭窄需手术的相对适应症为:(1)无症状的极重度AS(Vmax≥5m/s),手术风险较低。(2)无症状的严重AS,同时运动耐量降低或运动试验时血压降低。(3)有症状的重度AS,同时有平均跨瓣压降低和左心室射血分数降低,但小剂量多巴酚丁胺实验结果Vmax≥4m/s,或平均跨瓣压差增加至40mmHg以上。(4)有症状的低压差重度AS,EF≥50%,且临床表现、血流动力学及解剖结构支持AS为导致症状的因素。(5)行其他心脏手术的中度AS患者(Vmax 3.0~3.9m/s)。(6)无症状的严重主动脉瓣狭窄,病情进展快,手术风险低。
2.主动脉瓣狭窄手术策略——TAVI or SAVR(外科主动脉瓣膜置换术)?
2017年AHA/ACC瓣膜病指南指出,对于有症状的高危或中危患者,TAVI或SAVR的选择取决于患者个体手术风险、经济条件、意愿及偏好(I,A;IIa,B-R),目前的RCT研究表明此类患者SAVR与TAVI手术效果相当。当存在手术禁忌征且TAVI术后预期>12月时,推荐TAVI(I,A)。
在我国,2018年《中国经导管主动脉瓣置换术临床路径专家共识》指出,对于SAVR禁忌或高危的患者为TAVI手术绝对适应症。手术禁忌指:预期术后30天内发生死亡或不可逆合并症的风险>50%,或存在手术禁忌的合并症如胸部放射治疗后、肝功能衰竭、主动脉弥漫性严重钙化、极度虚弱等。
但TAVI手术因其手术方式的特殊性,有其独特的禁忌症:(1)左心室内血栓;(2)左心室流出道梗阻;(3)30天内心肌梗死;(4)左心室射血分数<20%(5) 严重右心室功能不全;(6)主动脉根部解剖形态不适合TAVI治疗;(7)存在其他严重合并症,即使纠正了瓣膜狭窄仍预期寿命不足1年。因此在选择术式时,应综合考虑患者病情,采取最能使患者受益的治疗方式。
3.TAVI手术的入路选择
目前TAVI手术的入路常见的有两种:经股动脉和经心尖。经股动脉入路,优点是1.风险相对低2.易控制出血。但缺点也很明显,股动脉—主动脉钙化严重或狭窄无法使用该路径,且易出现血管相关并发症。对此患者来说,患者右下肢血压不能测出,行超声检查提示双侧下肢粥样硬化斑块狭窄,经股动脉操作难度和风险均较大,故放弃此入路。经心尖入路优势:1.顺行入路,路径较短;2.避免了血管相关并发症;3.操作简便;4.入路较粗,可输送大尺寸鞘管。劣势为:1.创伤较股动脉大,需术者仔细缝合伤口;2.对心肌有损伤,出血风险相对较高。其他路径诸如:经颈动脉、经锁骨下,腋下动脉TAVI也有使用,但是采用较少。
威尼斯9499登录入口心脏外科 杨栩鹏