
威尼斯9499登录入口1月14日电(通讯员 赵亚参)2020年1月9日-1月12日,由我院药物临床试验机构办公室组织,国家药品监督管理局高级研修学院承办的“第107期药物临床试验质量管理规范(GCP)培训班”在集会厅召开。我院120余人参加培训,包括来自30个专业的主要研究者、辅助研究者、研究护士、技术人员、医疗器械科室人员、伦理委员以及其它临床研究相关的工作人员。

徐沪济副院长主持开幕式

国家药品监督管理局高级研修学院万征处长致开幕辞
我院临床试验机构负责人徐沪济副院长主持开幕式, 万征处长致开幕辞。我国目前正处于医疗药物改革创新的关键节点,一系列相关的政策法规出台,包括临床药物试验由资质认定改为备案制,是临床研究前所未有的大好机遇。GCP作为药物临床试验全过程的标准规范,其作用在于保证临床试验过程的规范和结果的科学,同时给予保护受试者的权益和安全保障。新的GCP法规即将出台,药监局高研院将进一步加强GCP的培训工作。徐副院长对于我院临床试验的成绩做出了肯定和鼓励,也强调了今后对各专业开展临床试验的高度要求,做临床试验必须严谨合规,保证试验的质量,并对参与药物临床试验的医护人员的职责、利弊、得失进行了深刻的分析,最后,他倡导我院医务人员以诚实务实、依法依规、恪守科学法规,、崇尚道德的精神来开展药物器械等的临床试验,进一步提升科室及医院的科研水平。

(由左至右依次为:熊玉卿、修清玉、孙晓春、蒋燕敏)

(由左至右依次为:黄瑾、胡蓓、姚晨)
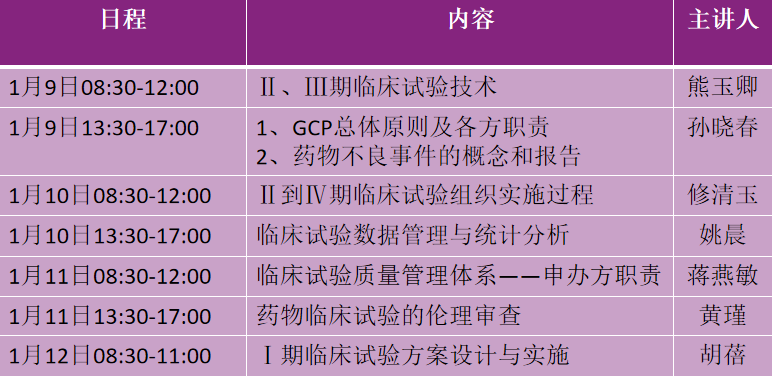
来自不同领域的具有丰富临床试验经验的7位资深专家分别从药政法规、I-III期临床试验设计和实施的关键要素、质量管理体系和各方职责、不良反应报告体系、临床试验统计方法、伦理审查原则等各个方面进行了培训。专家们以饱满的热情,风趣幽默的讲课方式对各个主题进行了由浅入深的细致讲解。会后参加培训人员也对此次培训做出了高度评价和反馈:“不出院门就能听到国家级专家授课,解决了我们在临床试验中遇到的难题”。
在培训会议结束后进行了在线电子答题GCP培训考试,合格者将于近期发放国家级GCP培训合格证书。